関連記事
がん治療薬に可能性! がん細胞が死を回避するメカニズムの一端を解明 神戸大など
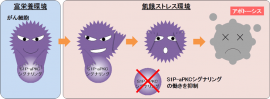
ストレスによるがん細胞死のブレーキ役として働く「S1P-aPKCシグナリング」。(画像: 神戸大学の発表資料より)[写真拡大]
がん細胞には死を回避するメカニズムが存在する。その一端を解明したのが、神戸大学大学院医学研究科とカリフォルニア大学サンディエゴ校の共同研究グループだ。
【こちらも】がんや肥満の創薬開発に役立つ細胞内ATP観察用蛍光センサー開発、早大など
研究グループは、がん細胞が飢餓などのストレスによるアポトーシス(死)を回避するさいのブレーキ役として、スフィンゴシン1-リン酸(S1P)とプロテインキナーゼC(PKC)という物質が直接作用していることを発見したのである。
通常、我々の身体の細胞は、日々様々な要因によってそのDNAが傷つけられ、その大半は修復される。もし修復不可能な場合は、細胞内にあるプログラムによって自殺することで、周辺の正常な細胞へ悪影響を与えないようにしている。
ところが、がん細胞は様々な方法で死を回避する能力を獲得しており、多くの細胞が死に至る飢餓などのストレス環境下でも生き続けることができるのである。
そこで研究グループは、がん細胞死のブレーキ役はがん細胞を生かす分子群の中に存在することを予測し、がん細胞の生存に関わることが知られている細胞内シグナルタンパク質である非典型プロテインキナーゼC(aPKC)に着目したのである。
上皮癌由来のがん細胞を用いてアポトーシス(死)の有無を観察したところ、aPKCの働きを抑えることでアポトーシスが誘導されたことから、aPKCはがん細胞のアポトーシスのブレーキ役として働いていることが判明した。
次にがん細胞死のブレーキ役としてのaPKCの活性制御メカニズムを明らかにするための実験を行い、スフィンゴシン1-リン酸(S1P)がaPKCに直接結合して活性化させることを突き止めたのである。さらに実験を進めS1PとC(PKC)が本来の能力を発揮なしければ、がん細胞をアポトーシス(死)から回避する能力が失われてしまうことも証明したのである。
がん治療に用いられる多くの抗がん剤はがん細胞のDNAをさらに損傷させてアポトーシスを起こさせるものが一般的だが、様々な回避能力を備えるがん細胞の全てをアポトーシスへ導くことは難しく、治療の妨げの一因となっていた。
今回の研究により、がん細胞アポトーシスのブレーキ役として、S1Pの直接作用によるaPKCの恒常的な活性化シグナリングを発見することができたのである。
研究グループは今後、この活性化シグナリングについて、組織・生体レベルでの検証を進め、将来的には、「がん細胞アポトーシスのブレーキ解除をターゲットとする新たな分子標的薬開発への早期展開が期待できる」としている。(記事:和田光生・記事一覧を見る)
スポンサードリンク
