関連記事
【QAあり】富士製薬工業、女性医療領域における既存品・新製品の貢献により増収増益 今期はさらなるスペシャリティファーマ化へ

【QAあり】富士製薬工業、女性医療領域における既存品・新製品の貢献により増収増益 今期はさらなるスペシャリティファーマ化へ[写真拡大]
本日のアジェンダ

岩井孝之氏(以下、岩井):本日はお忙しい中、富士製薬工業の2023年9月期決算説明会をご視聴いただき、ありがとうございます。どうぞよろしくお願いします。
本日は、2023年9月期の概要と中期経営計画の最終年度となる2024年9月期の業績予想についてご説明します。
2023年9月期連結決算ハイライト

2023年9月期は、これまで準備してきたことについて定量面・定性面で結果が出始めた年度となりました。女性医療領域製品が大きく伸長したことに加えて、タイの子会社であるOLICも連結ベースで業績に貢献し、2022年9月期比で増収増益となっています。
研究開発面においても大きな進捗がありました。まずは、女性医療領域において次のトップ製品と期待する「FSN-013」について、予定どおり日本での製造販売承認を申請しました。さらに9月には、バイオシミラー「ウステキヌマブBS」の製造販売承認を取得しています。
2023年9月期連結決算概要
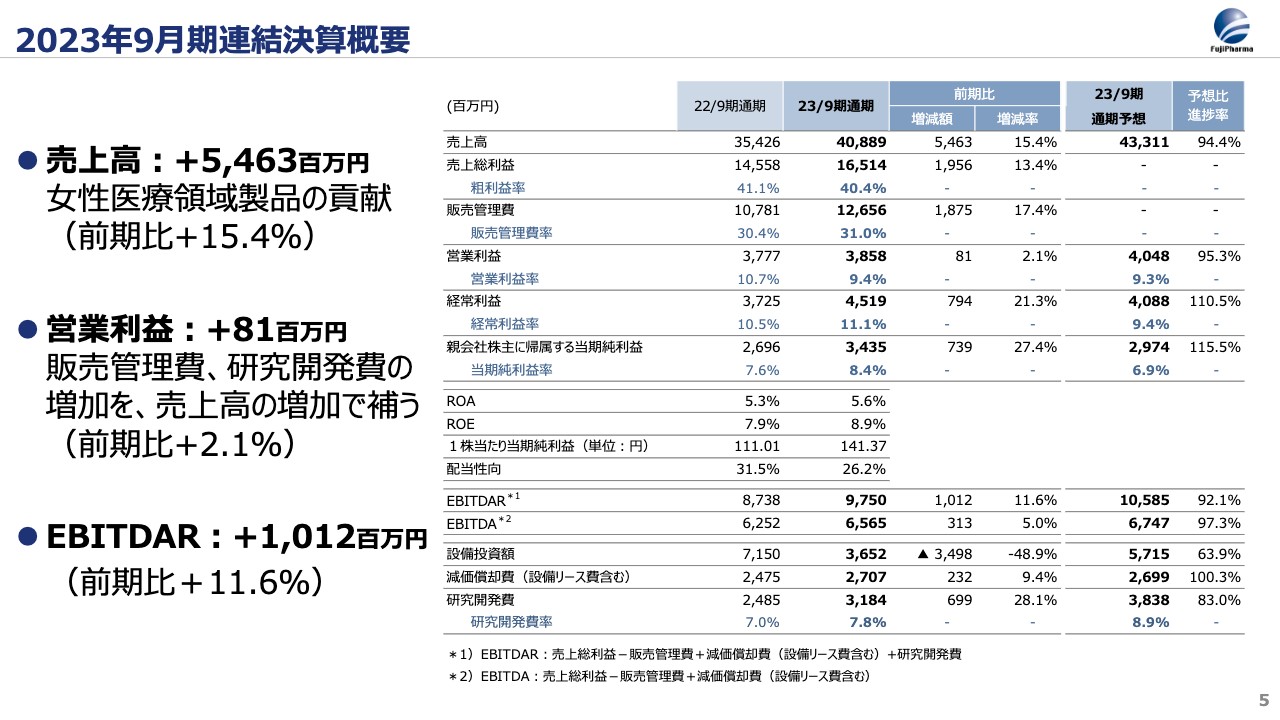
2023年9月期の連結決算について、女性医療領域、海外事業、研究開発に絞ってご説明します。まず、女性医療領域製品が着実に伸びたことで、売上高は前期比54億円増の409億円となり、過去最高を達成しました。また、営業利益は「FSN-013」の申請に伴う研究開発費の増加により、前期比8,000万円増にとどまりましたが、EBITDARは前期比10億円増加し、収益力は着実に増しています。
2023年9月期連結決算概要(前期比)
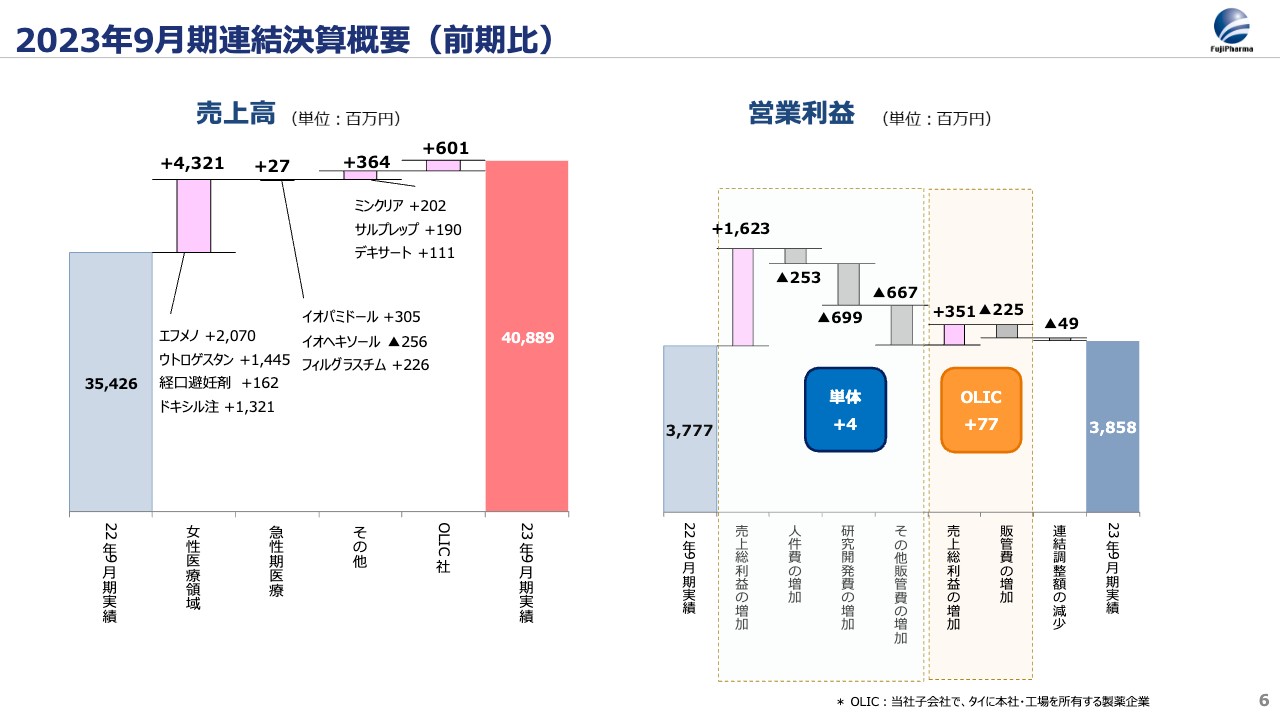
前期の増収ならびに収益力が高まった主な要因をご説明します。スライド左側のグラフは増収した54億円の内訳を記載したものです。各製品の売上高は、スライド12ページをご参照ください。
女性医療領域において、経口避妊薬は1億6,000万円の増加にとどまりました。一方、2021年9月に新薬の承認を取得した黄体ホルモン「エフメノカプセル」の売上高は通期で27億5,000万円となり、前期比で20億円増加しています。さらに、「ウトロゲスタン」も26億円の売上となり、前期比で14億円増加しました。当社の新薬が着実に市場に浸透していると感じています。
また、米国のバクスター社と提携して卵巣がんの治療薬「ドキシル」の販売を開始しました。こちらにより売上高は13億円増加しています。さらに、OLICは6億円増収し、最終的な連結売上高は409億円という結果になりました。
2023年9月期連結決算概要(予想比)
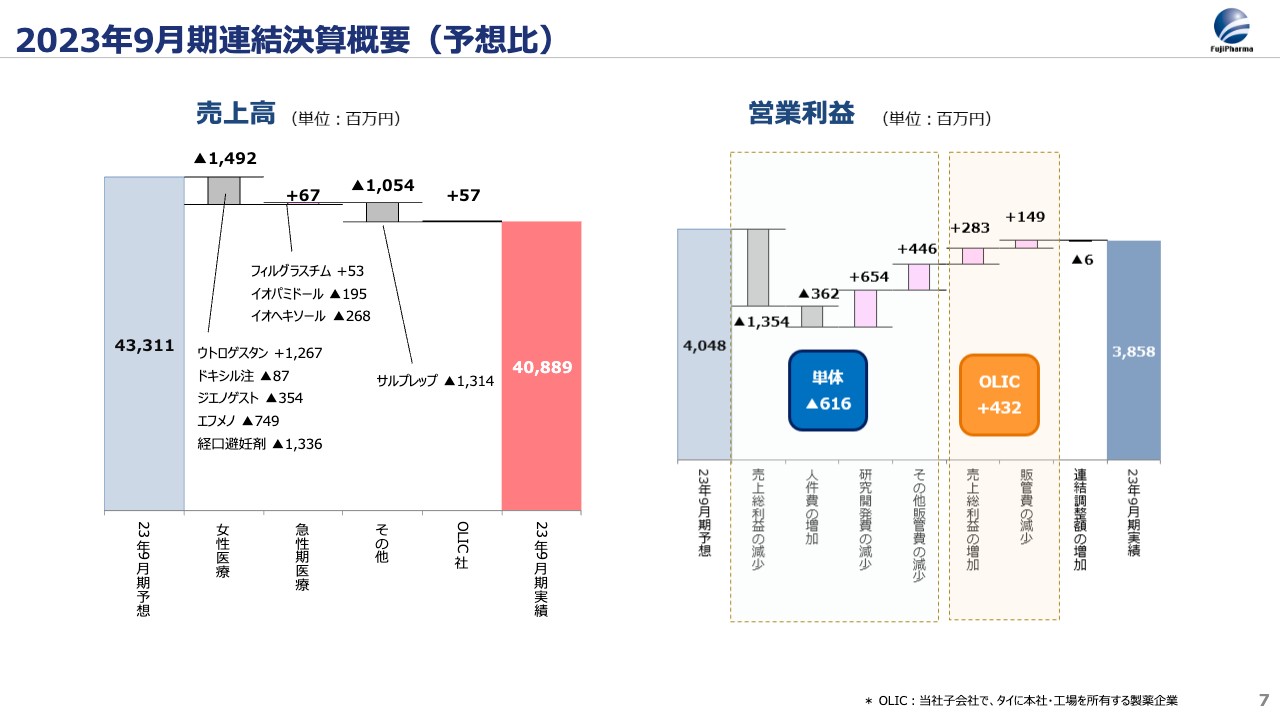
不妊症治療薬「ウトロゲスタン」は計画比で大きく伸びた一方、「エフメノカプセル」と経口避妊薬は計画を下回りました。
経口避妊薬が大きく未達となった理由は、同製剤を製造する新工場の立ち上げが遅れ、患者さまに必要な数量をお届けできなかったためです。現在は立ち上げが完了し、2024年9月期は十分な量を確実にお届けできる体制が整いました。
また、「エフメノカプセル」は前期比で20億円増と着実に市場浸透しましたが、計画比では7億5,000万円ほど遅れています。こちらはすでに対策を始めており、今期は患者さまにしっかりとお届けする予定です。
領域・剤形別売上高
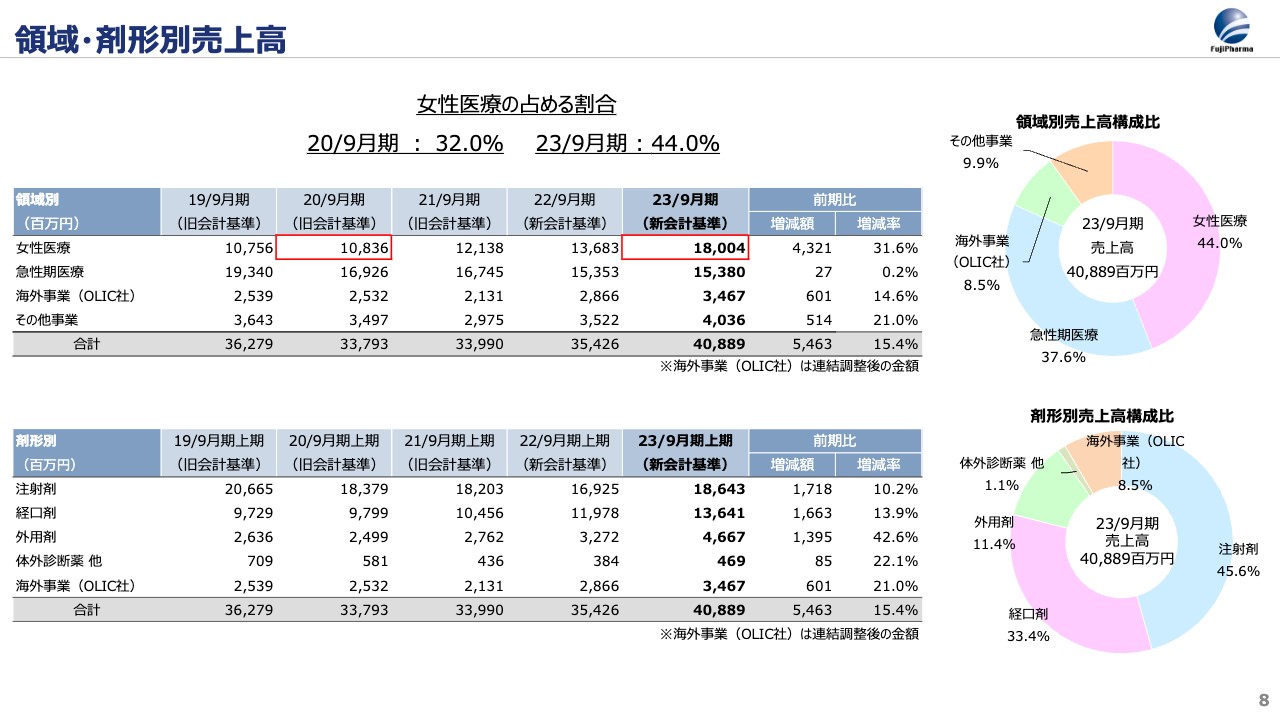
上段の表にあるとおり、中期経営計画の初年度である2020年9月期において、女性医療領域の売上高は108億円でした。当社全体の売上高に占める割合は32パーセントでしたが、2023年9月期は180億円まで伸び、全体に占める割合は44パーセントに拡大しました。この4年間で当社が女性医療領域に特化し、一層のスペシャリティファーマ化が進んだことが見て取れるかと思います。
また、造影剤を中心とする急性期医療領域でも、エッセンシャルな医薬品を提供する持続的な事業への転換を進めています。
下段の表は売上高の比率を剤形別に示したものですので、ご参照ください。
女性医療領域
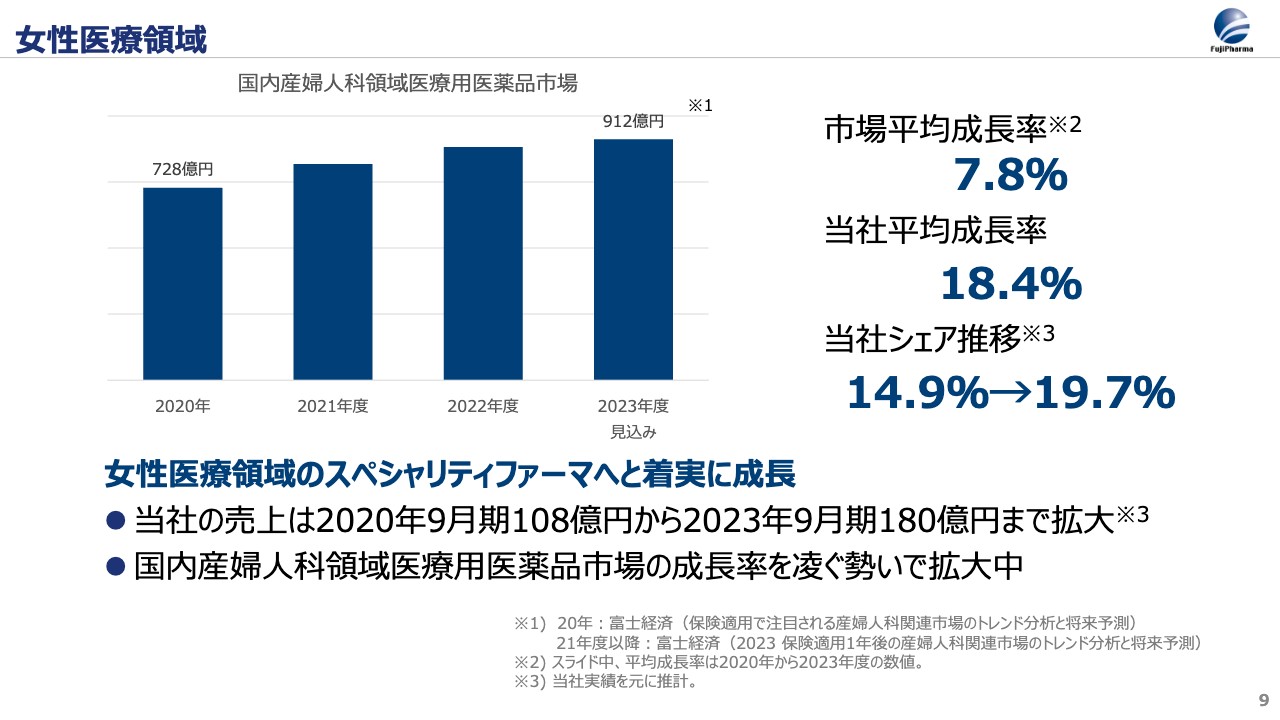
当社の女性医療領域事業について、国内での位置づけをお話しします。まず、2020年における国内全体の女性医療市場は728億円でしたが、2023年の見込みは912億となっています。
市場が拡大する中、当社は女性医療領域に特化し、ジェネリック企業からスペシャリティファーマへの転換を進めてきました。2023年9月期はその結果が数字に表れはじめ、市場平均成長率8パーセントに対して、当社の女性医療領域は18パーセントの成長となりました。市場におけるシェア率も、15パーセントから20パーセントに増加しています。
市場の拡大要因は、大きく2つあります。1つは、従来に増して女性の社会進出が進み、健康意識が高まっていることです。もう1つは、不妊治療の保険適用が挙げられます。
当社は幅広い年代の患者さまが必要とする医薬品を取り揃え、新薬とジェネリックの両方を提供してきました。患者さまや医療機関のみなさまに貢献してきた結果が、このような数字に表れていると考えています。
女性医療・急性期医療売上高
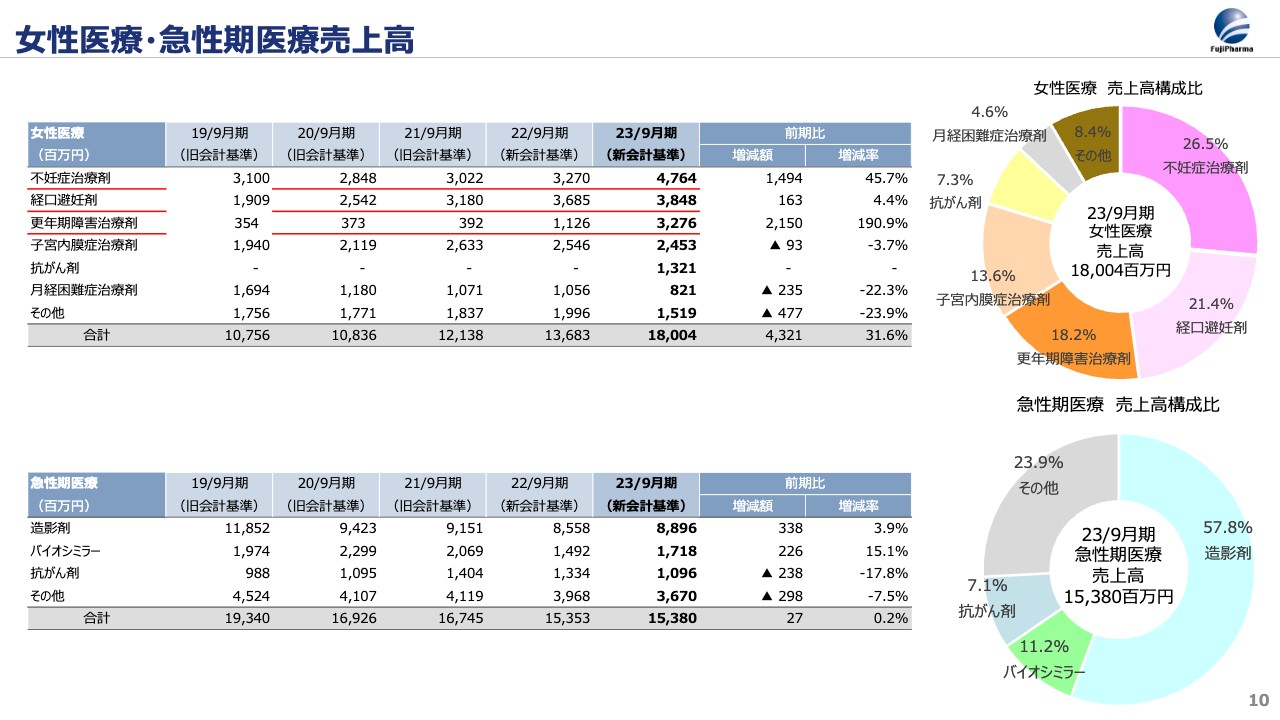
上段の表は、女性医療領域の売上高の内訳をまとめたものです。2020年9月期と2023年9月期を比較すると、不妊治療剤は28億円から47億円に増加し、経口避妊剤も25億円から38億円に伸びています。更年期障害治療剤については、2021年末から「エフメノカプセル」を販売開始したことで、4億円から32億円にまで成長しました。こちらは患者さまに必要とされる製品を、しっかりとお届けできた結果と考えています。
昨年、当社製品において大きく伸びた領域が、不妊症治療剤の市場と更年期障害の治療剤の市場です。この2つの領域における当社の状況については、重ねてご説明したいと思います。
なお、下段の表は急性期医療領域の売上高です。造影剤を中心とする急性期医療の分野でも、持続的な事業への転換が着実に進んでいます。
当社女性医療領域製剤の中でも不妊症治療剤・ 更年障害治療剤が大きく拡大
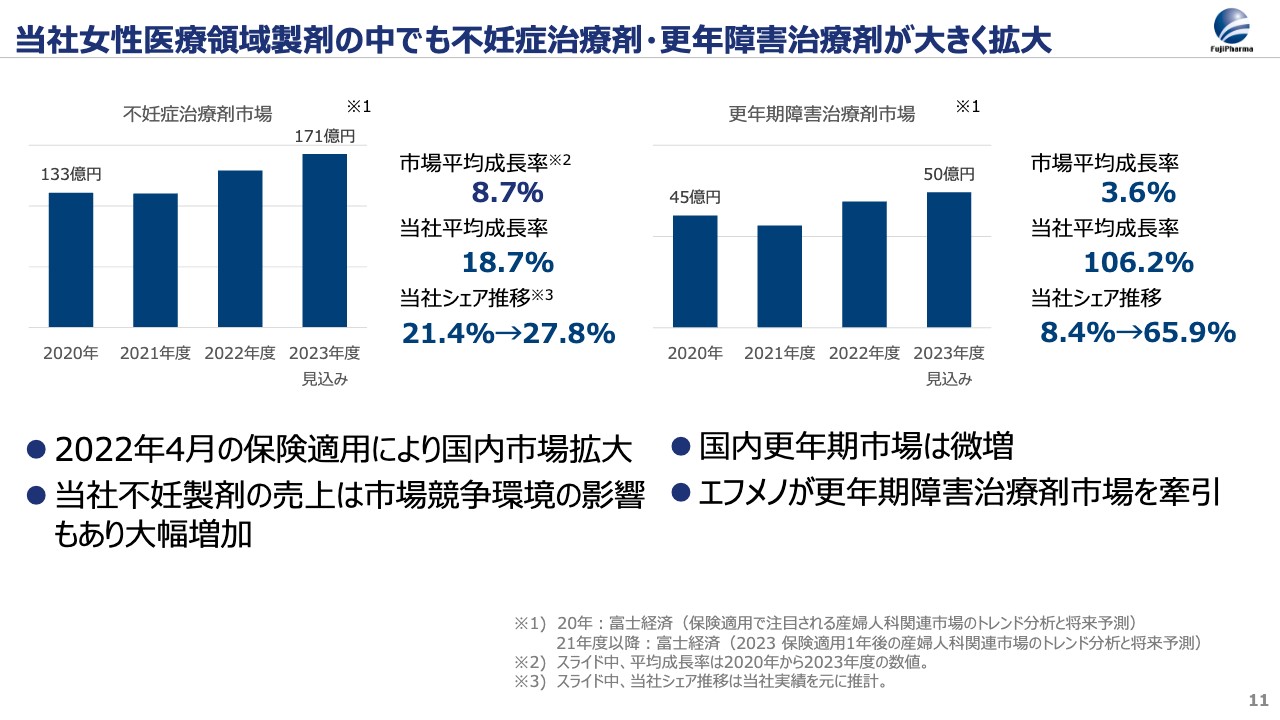
2023年9月期は、不妊症と更年期障害の治療剤が大きく拡大しました。スライド左側の棒グラフは不妊症治療剤市場の成長を表すものです。2022年から保険適用となった影響で、全体市場は2020年の133億円から2023年には171億円に拡大し、平均成長率は9パーセントとなっています。
当社製品においても、この4年間の平均成長率は19パーセントと大きく伸び、シェア率は21パーセントから28パーセントまで拡大しました。市場の成長に加えて、患者さまが必要とする医薬品を確実にお届けできた結果と考えています。
スライド右側の棒グラフは更年期障害治療剤市場の成長を表しています。2023年の全体市場は50億円と、過去4年間における成長は限定的です。しかし、当社は2021年に「エフメノカプセル」の承認を取得したことで、この分野における存在感がかなり大きくなっています。更年期障害治療剤の市場は、当社が今後一層貢献していくべき市場と考えています。後ほど詳細をお伝えします。
売上上位15製品のうち9製品が女性医療領域
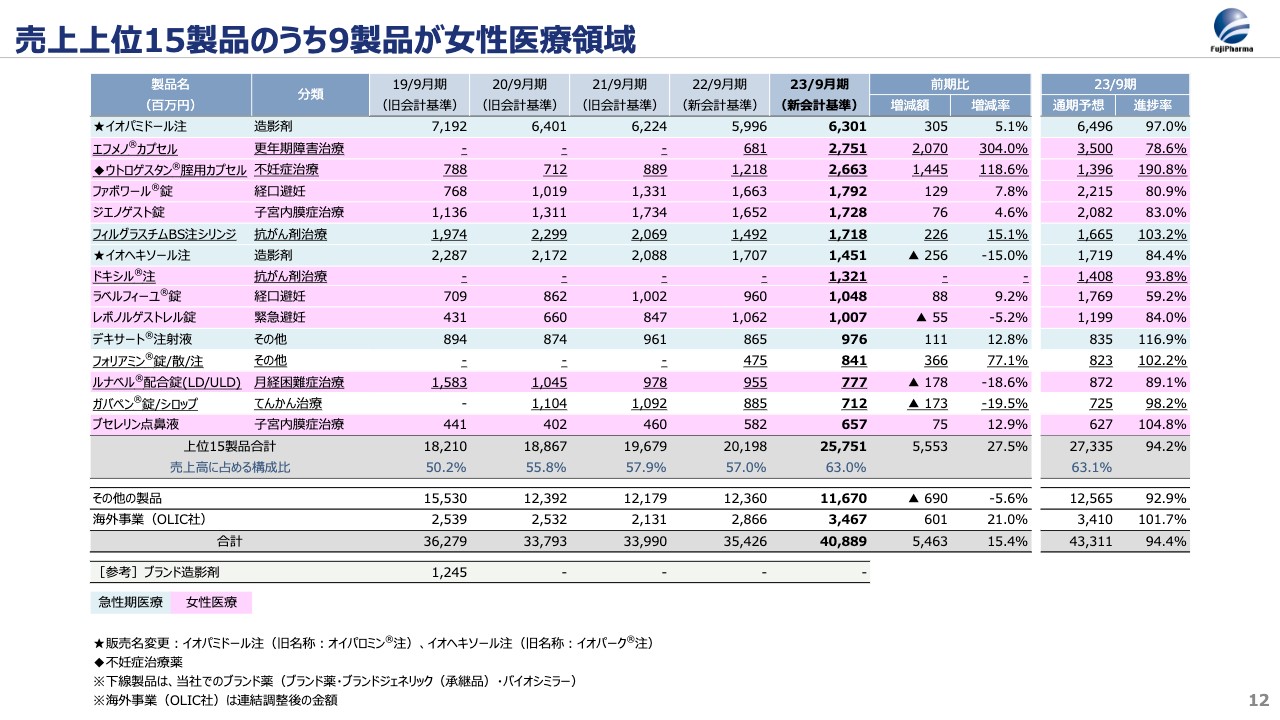
当社の売上上位15製品のうち、9つが女性医療領域の製品となっています。この結果からも、当社のスペシャリティファーマ化が進んでいることがご理解いただけるかと思います。
海外事業

海外事業は、ASEANと米国事業に分けてご説明します。まず、ASEANは市場の拡大に伴い、従来のOLIC受託ビジネスが順調に伸びています。円安効果もあり、前期比21パーセントの増加となりました。
また、4月から「FSN-013」と同じく、E4という新しい卵胞ホルモンを配合したピルの販売を開始しました。右側の写真は、バンコクで開催したローンチイベントの様子です。タイ国内の先生方が200名ほど参加され、この製品への関心の高さが窺えるイベントとなりました。
一方、米国事業は、OLICと富士製薬工業本体の双方で具体的な案件が進み始めたところです。OLICでは米国向け注射製剤の受託が進んでおり、今年3月にFDAの承認前査察を完了しました。また、日本では米国のパートナー会社と提携し、昨年から女性医療領域での新薬開発に着手しています。海外事業の進捗は中期経営計画から若干遅れているものの、いずれも具体的な案件が進行している状況です。
研究開発関連・新製品トピックス

次に、新製品のトピックスです。まず、当社の女性医療領域事業において次のトップ製品となる月経困難症治療薬「FSN-013」について、今年10月に販売承認申請を行いました。また、バイオシミラー「ウステキヌマブBS」と、ジェネリックの2製品については承認取得となりました。
新製品としては、今後より注力していく予定の更年期障害治療薬において、エストラジオール錠「F」の発売を開始しました。
これらの製品の2024年9月期における定量的なインパクトは、後ほど事業計画説明の中でお話しします。また、月経困難症治療薬として申請した「FSN-013」についても、製品概要や市場に関して、今期計画の中でもう少し詳しくお話しします。
2023年9月期連結貸借対照表概要
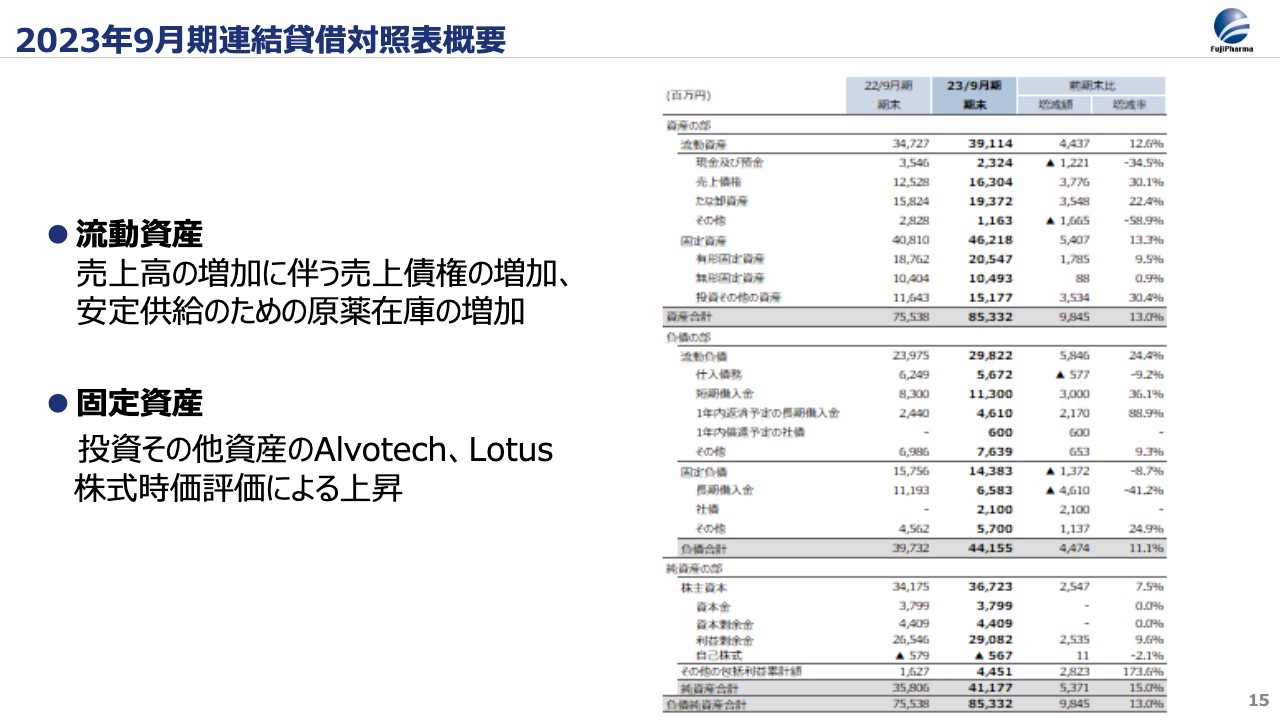
こちらは2023年9月期の貸借対照表です。流動資産と固定資産について、それぞれスライドに記載の理由で、合計100億円増加しました。
2023年9月期連結キャッシュ・フロー計算書概要

続いて、キャッシュ・フローです。営業キャッシュ・フローは前期比で25億円増加し、投資キャッシュ・フローは60億円の増加となりました。財務キャッシュ・フローは30億円減少しています。
2024年9月期連結業績予想ハイライト

ここからは、2024年9月期の連結業績予想をお話しします。2023年9月期は、「これまで準備してきたことについて、ようやく結果が出始めた年」とお伝えしましたが、中期経営計画の最終年度となる2024年9月期は、より具体的な成果が期待できる年だと考えています。
2024年9月期連結業績予想
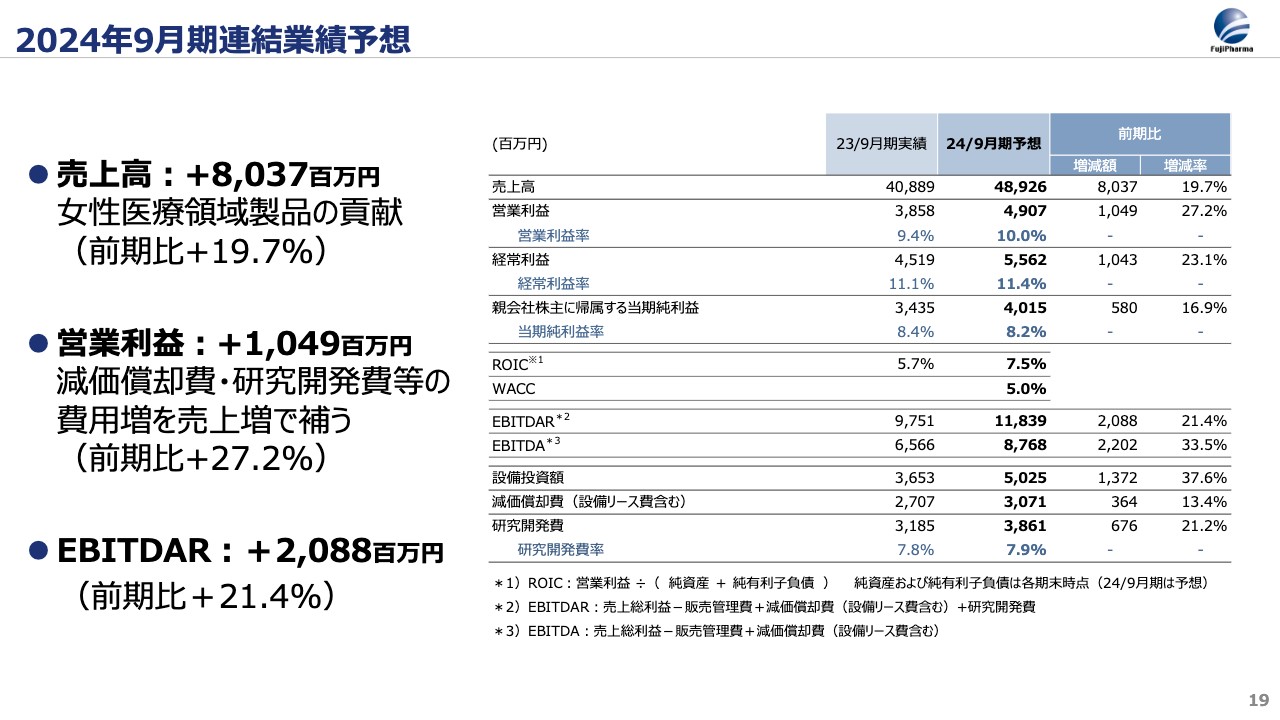
2024年9月期の業績予想です。まず、売上高は女性医療領域の製品を中心に伸びる見込みで、前期比80億円増の490億円、営業利益は10億円増の49億円を計画しています。これらに基づくEBITDARとEBITDAは、スライドに記載のとおりそれぞれ118億円と87億円で、2023年9月期に比べて20億円の増加となります。
お伝えしたとおり、今期事業計画達成の鍵は当社が女性医療領域で着実に患者さまに貢献していくことです。そこで今日はこの点を重点的に今期の計画内容をお伝えしたいと思います。
2024年9月期連結業績予想
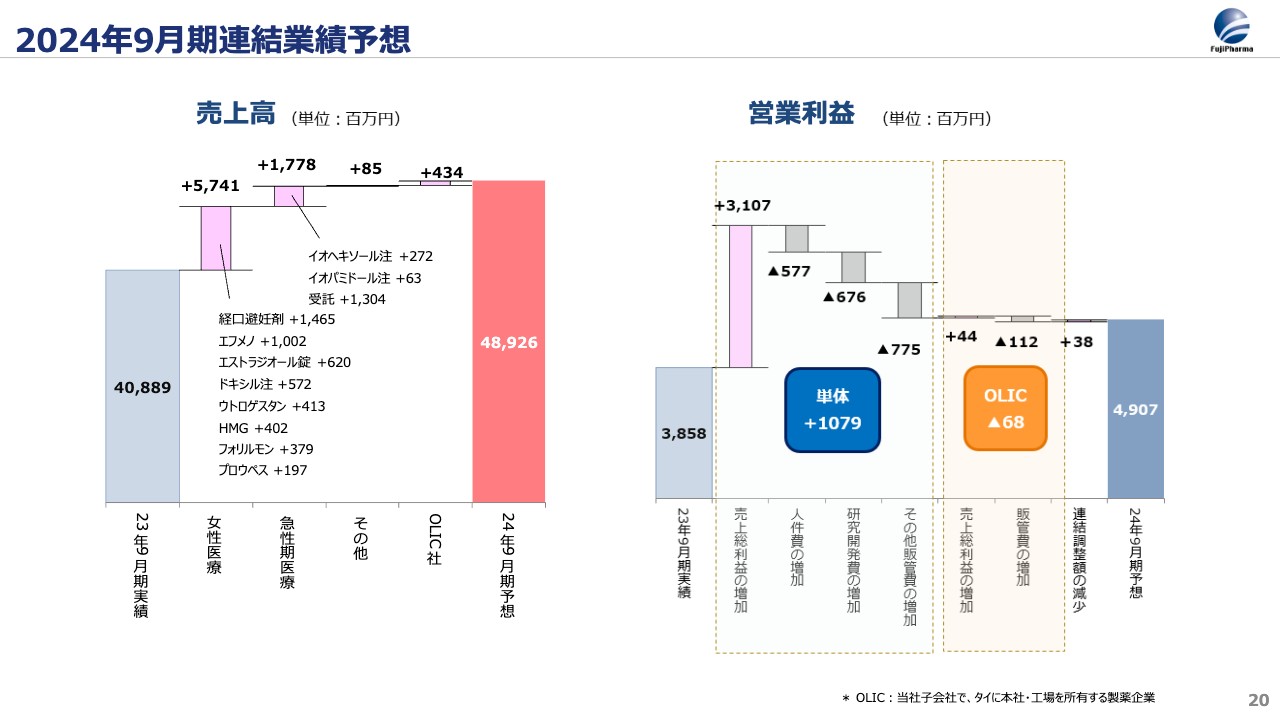
スライド左のグラフは、先ほどお伝えした売上高が80億円増加したことの内訳です。女性医療領域は57億円増えていますが、この内訳は大きく3つに分かれます。
1つ目は経口避妊薬です。前期は新工場の立ち上げが遅れたために1.6億円の増加にとどまりましたが、今期の2024年9月期は新工場での生産が本格化します。前期とは異なり、供給を制限することなく必要な数量を本当に必要とされる患者さまへ届ける体制が整います。そのため、経口避妊薬の分野では確実な増加を見込んでいます。
2つ目は更年期障害の市場における製品です。更年期障害の治療方法の1つのホルモン補充療法では、卵胞ホルモンと黄体ホルモンと呼ばれる2つのホルモンが使われます。スライド14ページで、先期に新製品の「エストラジオール錠」を発売開始したとお伝えしましたが、これがホルモン補充療法で使われる卵胞ホルモンです。今期はこちらの「エストラジオール錠」の一定量の貢献が見込まれます。
また、もう一方の黄体ホルモンは「エフメノカプセル」です。前期は計画比で約7.5億円のビハインドでしたが、医療機関の先生方への理解が着実に進んでいます。医療現場で患者さまへの処方が着実に増えており、約10億円の増加が見込まれる状況となってきました。
3つ目は不妊症治療の製剤群です。保険適用後は、不妊治療に使われる主力製品の「ウトロゲスタン」をはじめ、「HMG」や「フォリルモン」が従来以上に患者さまから必要とされています。今期はこれら製品群の増加も見込んでいます。
次に、売上高のグラフ中央にある急性期医療の17億円増加部分の内訳をご覧ください。富山工場で約3年にわたり取り組んできた新規の受託ビジネスが今期から具体化します。また、ASEANの市場回復に伴い、OLICの新規CMO事業も順調に進んでいます。
これらの結果、前期比80億円増の490億円を計画しています。
領域別売上高予想
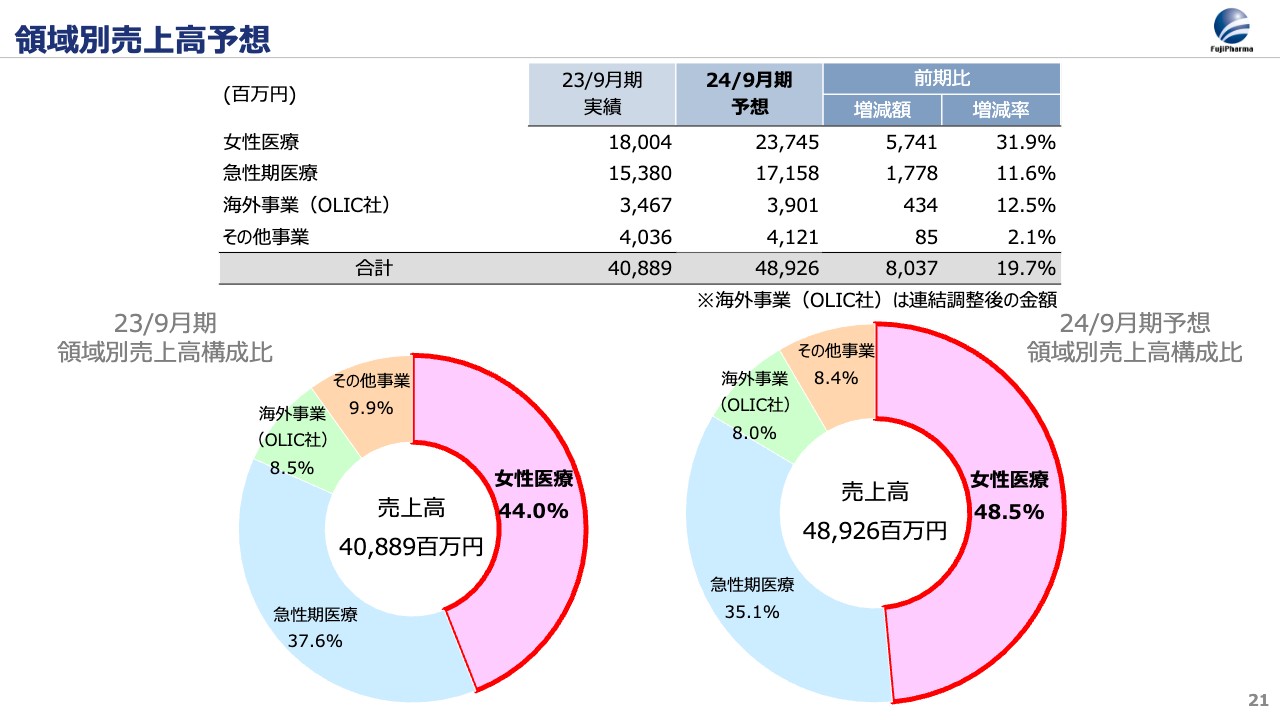
今お伝えしたことをもう一度領域別に整理すると、スライドの表のようになります。女性医療は、前期の180億円に対して57億円増加し、通年の合計で237億円となっています。また、急性期医療が171億円、海外が39億円となり、連結売上高は490億円となります。
2023年9月期は女性医療の当社全体に占める割合は44パーセントでしたが、今期はさらに増加して48パーセントを超える見込みです。ますますこの分野で当社の存在感が高まってきていると考えています。
2020年9月期実績と2024年9月期予想の比較
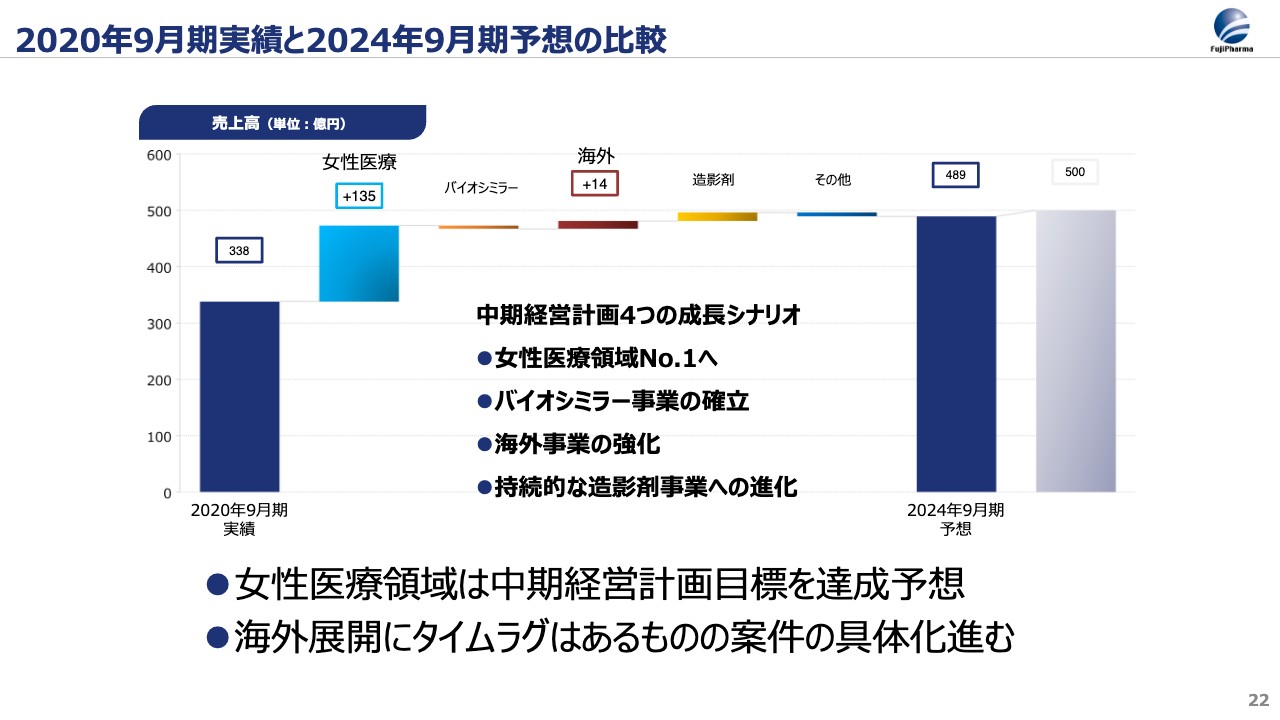
女性医療領域を中心にお伝えしましたが、こちらを4年前に発表した中期経営計画の最終年度と比較するとスライドのようになります。内訳は当時の計画と若干異なりますが、女性医療領域が大きく伸びることで、おおむね同等の連結売上高、営業利益を計画しています。
この後のスライドでご説明しますが、4年前の売上高は108億円であり、女性医療領域を中心に最終年度には倍の200億円にするとお伝えしていました。しかし、この4年間で着実に新しい製品ポートフォリオを揃え、少し遅れましたが富山での供給体制も整ったことから、今期は女性医療領域を237億円と計画しています。
2024年9月期 女性医療領域
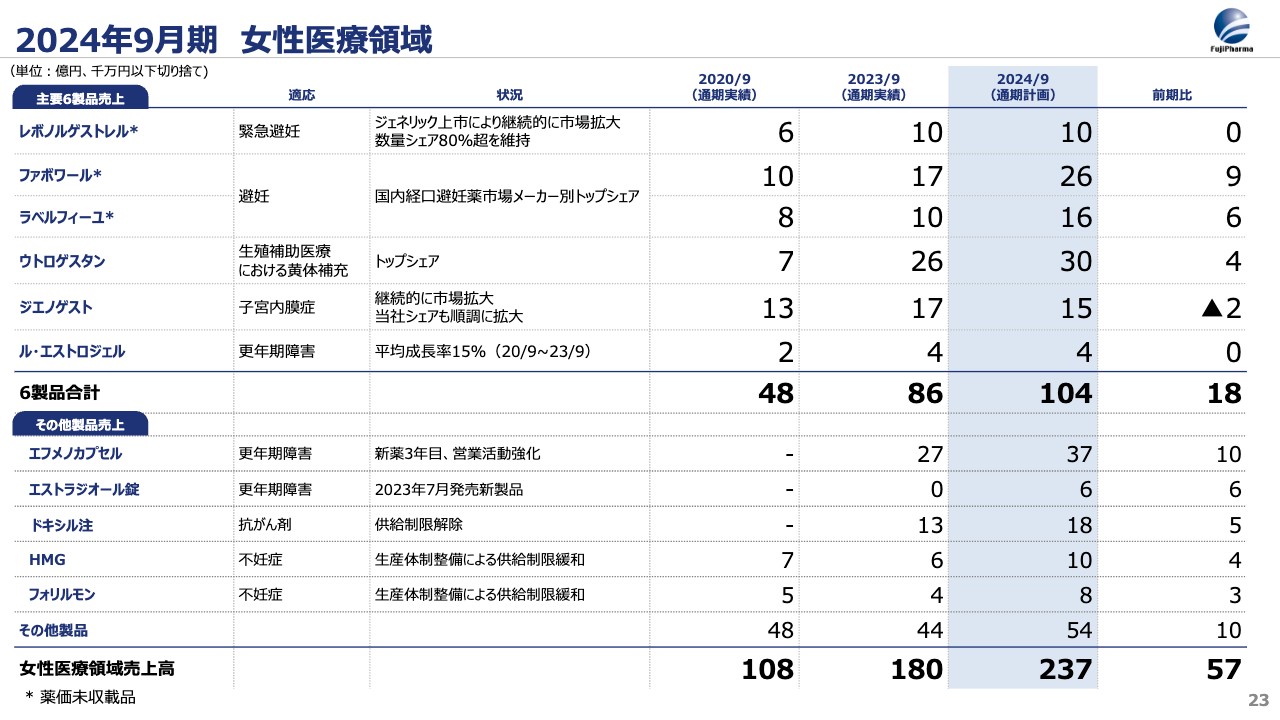
今期における定量面の事業計画です。当社の鍵は女性医療領域で十分に患者さまへ医薬品を届けられるかにかかっています。この点を中計発表時と比較してご説明します。
上段は、これまで中期経営計画発表時から扱っている主要6製品の実績と計画値です。4年前の2020年9月期当時の売上高は100億円で、中計最終年度には倍の200億円にするとお伝えしました。
当時の内訳は、スライドの一番下の段にあるその他のところで横ばいです。一方、主要6製品の50億円を、倍の100億円にする計画でした。また、当時はなかった新規製品で50億円を足し、全体として200億円とお伝えしました。
主要6製品に関しては、前期に富山の新工場が立ち上がり、今後は経口避妊薬の伸びも期待できます。また、「エフメノカプセル」「エストラジオール錠」「ドキシル注」は新規製品で、4年前にはありませんでした。医療現場や患者さまに届ける体制が十分に整ったことなどから、前期にはすでに定量結果が出て「エフメノカプセル」「ドキシル注」2製品の合計で40億円となっています。
今期は先にお伝えした施策を進めます。この女性医療領域を中心に、今期は着実に伸ばしていく計画です。
新製品開発(パイプライン)
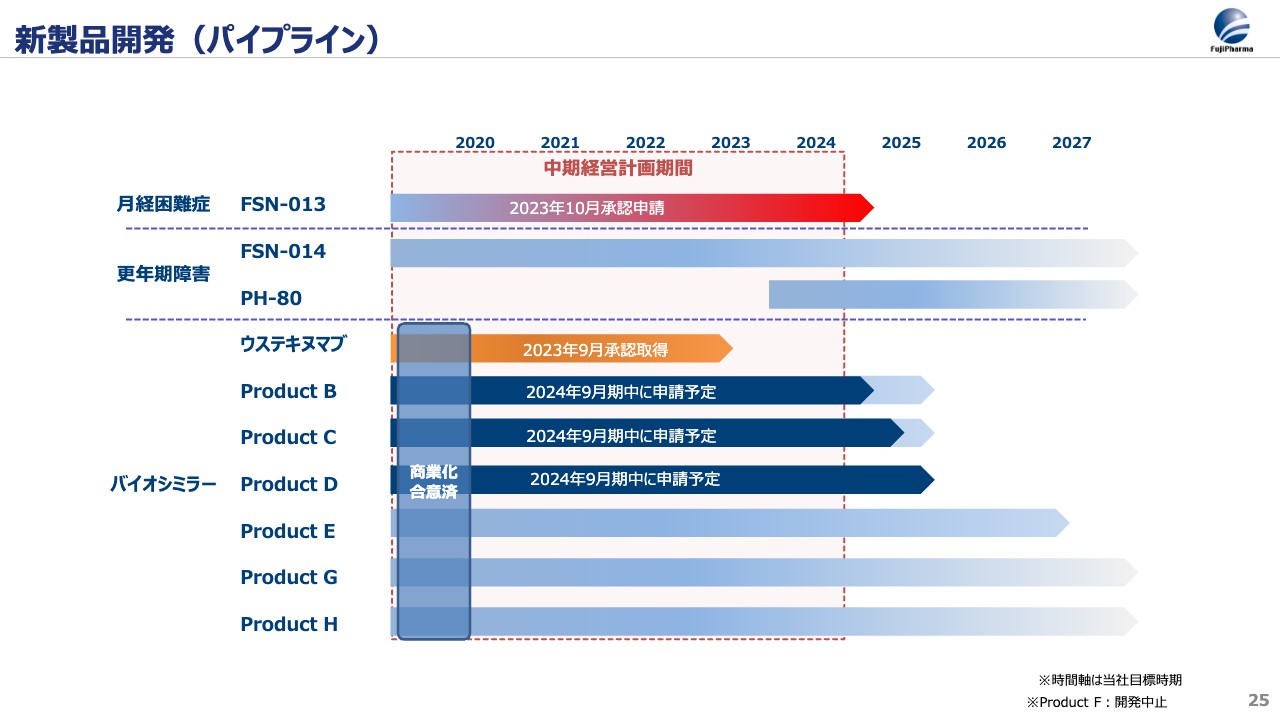
次に、新製品と海外事業における今期の計画をお伝えします。スライドは、新製品開発のパイプラインである、月経困難症の治療薬、更年期障害の治療薬、バイオシミラーです。今までは別々に示していましたが、今回はバイオシミラーもあわせて記載しています。これら3つそれぞれについてお伝えします。
まず、「FSN-013」「PH-80」については、研究開発本部副本部長の長縄が説明を行います。市上に関して質問があれば、Q&Aの中で別途ご説明したいと思います。
新製品開発(パイプライン) - 月経困難症(FSN-013)①

長縄正之氏(以下、長縄):研究開発本部の長縄です。「FSN-013」について新たな進捗がありましたので、ご説明します。こちらは、次世代の月経困難症治療剤として開発を進めてきましたが、データの解析が終わり、今年10月に月経困難症の適応で承認申請を行いました。これから当局と審査を進めていきます。
本日は、特徴の1つである「エステトロール」の血液凝固系について、興味深い結果が得られたため、次のスライドでご説明します。
新製品開発(パイプライン) - 月経困難症(FSN-013)②
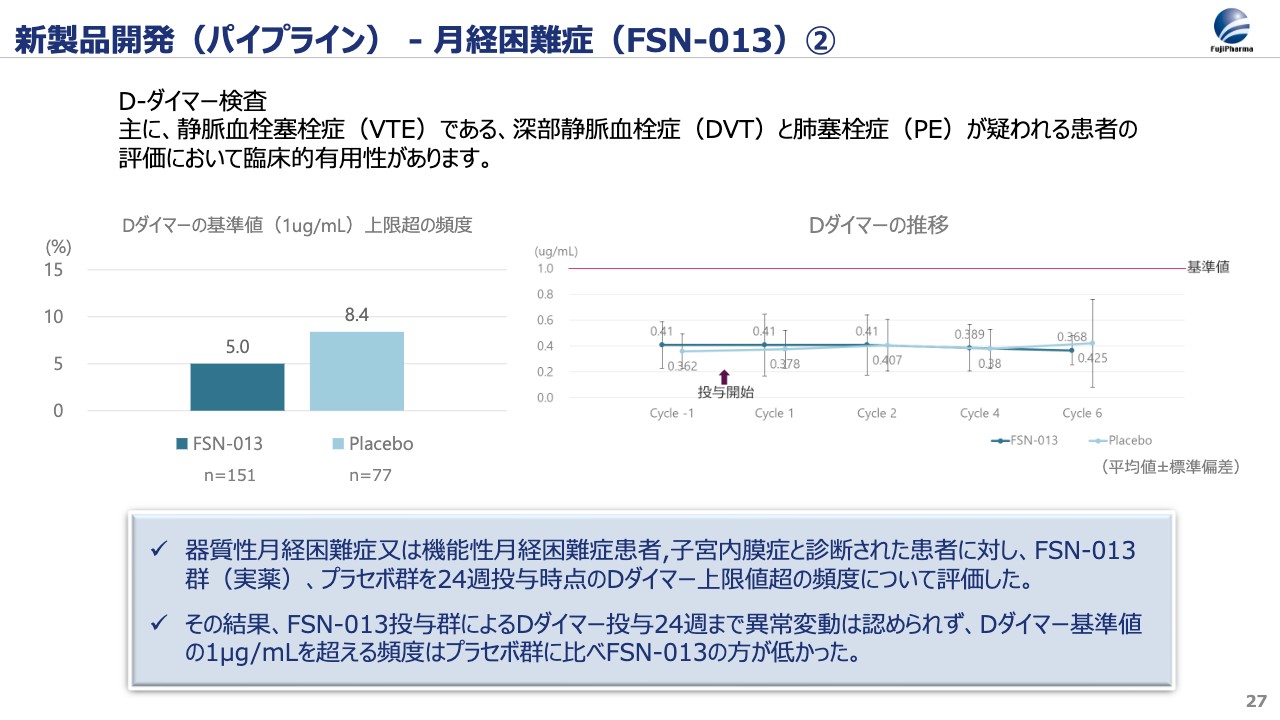
スライドは、器質性月経困難症・機能性月経困難症、子宮内膜症の患者さまに対して「FSN-013」またはプラセボを投与した際の、Dダイマーの推移と上限値を超える頻度を示したものです。
Dダイマーは、主に静脈血栓塞栓症(VTE)である、深部静脈血栓症(DVT)と肺塞栓症(PE)が疑われる患者さまの評価において臨床的有用性があります。
スライド右側の図がDダイマーの推移、左側がDダイマーの基準値の上限を超えた頻度を示しています。右側の図では、投与前のCycle -1からCycle 6が示されています。Cycleは1Cycleを28日とカウントするため、24週間ということです。結果は、平均値と標準偏差で示しており、グラフ上部の赤線が基準値です。
結果についてです。濃い青色の線の「FSN-013」を投与した群で、投与前から基準値内にあり、値は変化が見られず平坦に推移しています。
また、薄い青色の線がプラセボ群です。こちらも投与前から変化がなく推移しています。「FSN-013」とプラセボを見比べても同程度の推移があるため、薬による影響がほとんど見られないことがわかります。
一方、スライド左側の図は、1マイクログラムパーミリリットルの上限値を超えた割合の解析結果です。「FSN-013」は5.0パーセントなのに対して、プラセボは8.4パーセントとなっています。したがって、「FSN-013」は、プラセボに対して値が低いという結果が得られました。他の血液凝固マーカーに対する影響もほとんどなく、本剤の血液凝固系に対する影響が少ないことが示唆されています。
従来の月経困難症治療薬で使用されている卵胞ホルモンは、主に「エチニルエストラジオール」です。これを含む配合剤でよく報告されている血栓症の副作用が、減少すると期待しています。
新製品開発(パイプライン) - 月経困難症(FSN-013)③
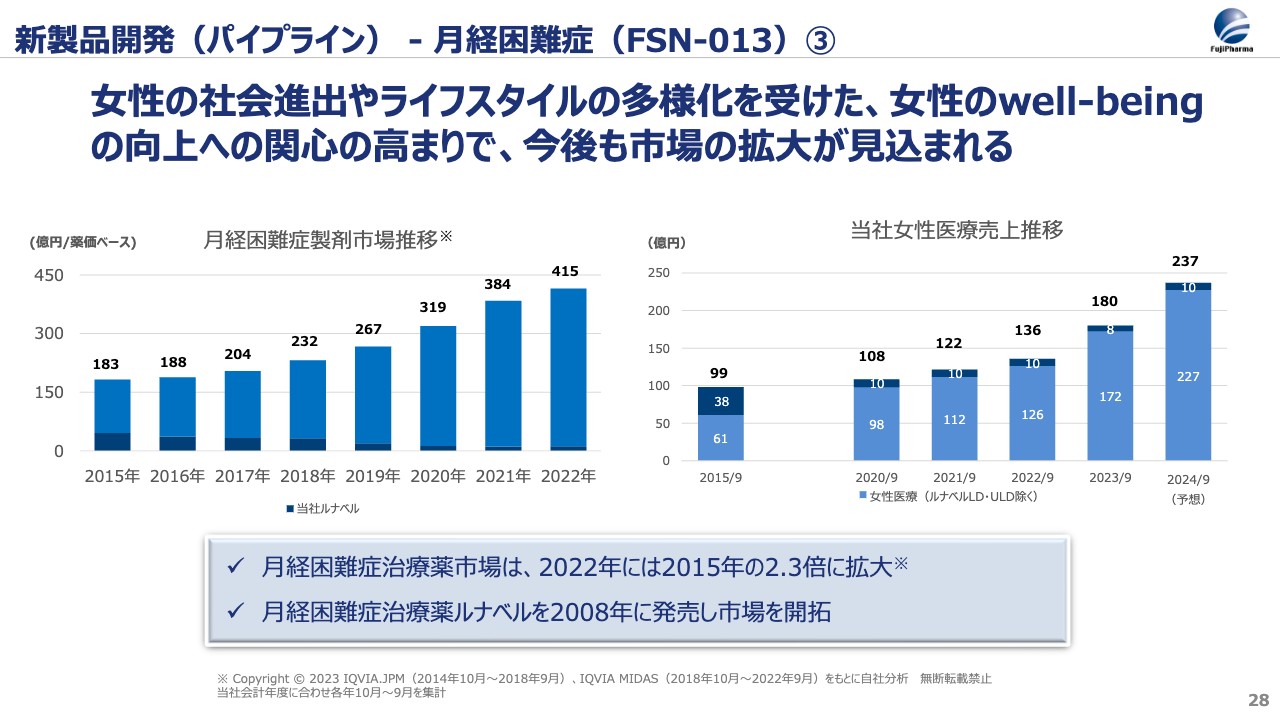
岩井:続いて、「FSN-013」を投入していく月経困難症の市場と、その中における当社のケイパビリティに関してお伝えします。女性の社会進出がますます進んでおり、ライフスタイルの多様化や健康への関心も増加しています。これにより、月経困難症治療剤の市場は大きく拡大し、2015年の183億円から、2022年には倍以上の415億円になっています。
この市場に当社が「FSN-013」を投入していきますが、実はこの市場において、2008年から実績があります。2008年にノーベルファーマの月経困難症治療薬「ルナベル」を併売しています。
「ルナベル」における当社販売分の売上は、ピーク時で約40億円でした。その後「ルナベル」のジェネリックが他社から販売されたことで、現在の当社における「ルナベル」の売上高は大きく減少しています。
しかし、これまでの「ルナベル」の販売を通して得られた月経困難症治療薬市場における経験や実績があります。さらに、先ほど長縄がお伝えしたとおり、血液凝固系への影響が少ないという製品の特徴を活かして「FSN-013」を当社の次のトップ製品にしていくことが、来期以降の重要な取り組み事項となっています。
新製品開発(パイプライン) - 更年期障害

次に、更年期障害治療剤についてお伝えします。まず、当社の考え方です。当社はこの分野のホルモン補充療法として、スライドに記載のとおり「ル・エストロジェル」「エストラジオール錠」という卵胞ホルモンをすでに販売しています。
これと同時に黄体ホルモンも使用されるわけですが、黄体ホルモンはすでにご説明を行った「エフメノカプセル」で、2021年から患者さまへ提供しています。
スライド11ページで「更年期障害の治療薬市場の成長は現在のところ限定的」とお伝えしましたが、前のスライドでは、この10年近くで月経困難症治療薬が大きく伸びてきているとお伝えしました。
月経困難症の市場で使われるホルモン製剤の使用が拡大していくことにより、更年期障害の治療においてもホルモン補充療法の市場が拡大してくると考えています。
一方で、更年期における症状は、スライド上段に書いているように多種多様で、さまざまな悩みを抱えている患者さまがいます。このように多くの悩みを解決できる製品を、ホルモン製剤に限らず幅広く提供していくことが当社の使命と考えています。
現在、「FSN-013」と成分を同じくするE4という新しい卵胞ホルモンを使った新しいホルモン補充療法の医薬品を開発中です。フェーズ1が終了しており、今後の開発方針について検討を進めているところです。
これらのホルモン製剤に加え、非ホルモン製剤と医科向けサプリの開発も進めています。今年9月に、米国のVistagen Therapeuticsという会社と独占交渉の契約を締結した非ホルモン製剤「PH-80」の製品概要に関して、長縄のほうから説明を行います。
新製品開発(パイプライン) - 更年期障害(PH80)

長縄:新しい治療剤の「PH-80」の概要についてご説明します。こちらは米国のVistagen Therapeuticsが開発中の鼻腔内スプレー剤です。当社は2023年9月に、日本における開発権や商業化における独占交渉権の合意を得ています。
この薬剤は、鼻腔内の化学ニューロンを活性化することにより、更年期に伴う血管運動神経症状であるHot flushに対して治療効果を発揮すると考えています。
36例で行ったフェーズ2試験、プラセボ対象の二重盲検試験ですが、投与から1週間でHot flushが有意に減少し、その後も維持できたという結果が得られています。また、治療期間中のHot flushの重症度、あるいは機能障害および発汗も有意に減少したという報告がありました。
また、安全性について重篤な有害事象はありません。有害事象のプロファイルは「PH-80」とプラス5との間で同等という結果が得られており、認容性の高い薬剤であることが示されました。
米国でこれから開発を進めていくことになっていますので、当社では「PH-80」のデータの精査を行い、日本での開発を検討します。進捗があり次第、あらためてご説明します。
岩井:当社では、更年期障害の治療剤は、今後一層注目して取り組むべき市場であると考えています。ホルモン補充療法に関しては、これから使用が増えていくと予測される一方、多様な治療選択肢の提供も重要であると考えています。この両面から、この市場に関してしっかり取り組んでいきたいと思っています。
新製品開発(パイプライン) - バイオシミラー
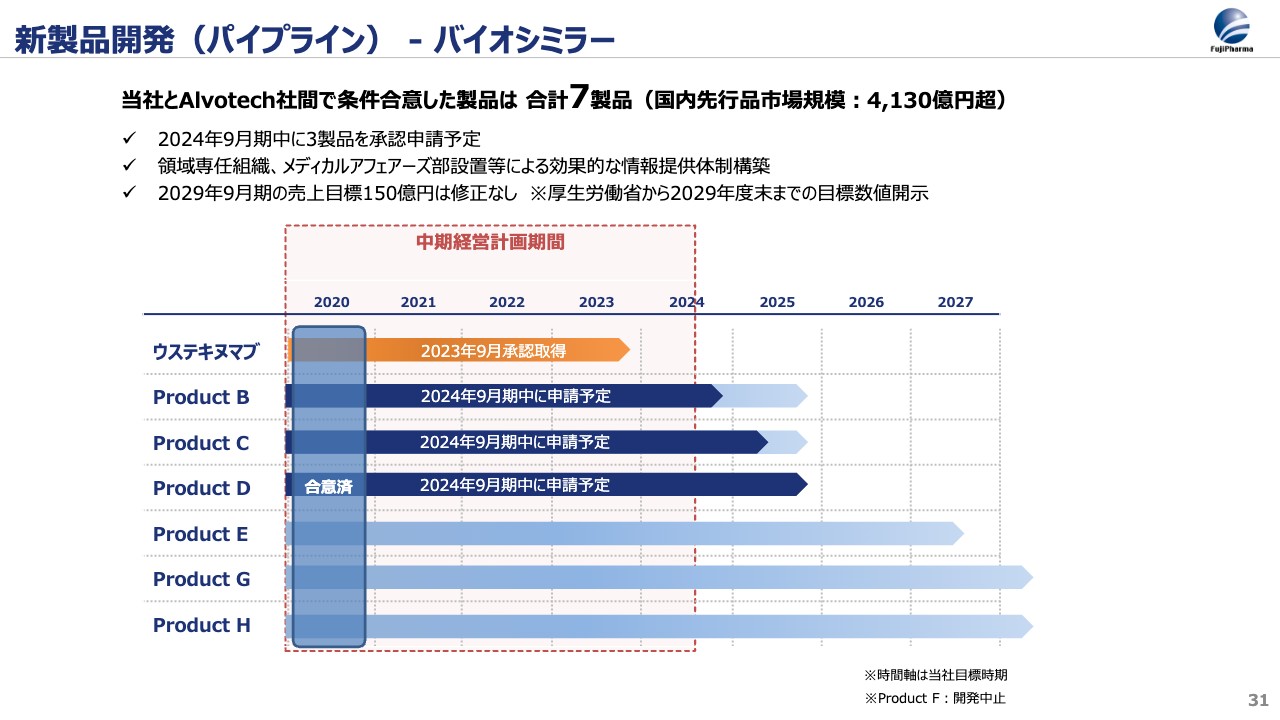
バイオシミラーの開発パイプラインについて、従来からお示ししているスライドです。7製品に関して、アイスランドのAlvotech社と日本向けの開発契約を締結し、現在開発を進めています。このスライドを初めて提示してからずいぶん時間が経過しましたが、その後計画どおり具体化したのが、冒頭にもお伝えしました今年9月の「ウステキヌマブBS」の承認取得です。
これに続く製品については、今期中に3製剤に関する承認申請を計画し、Alvotech社と共同で進めているところです。これらの製品を確実に患者さまにお届けしていくことを念頭に、少し新しい領域も入ってきますので、領域専任の組織やメディカルアフェアーズ部門を10月に新たに設置し、効果的な情報提供体制を構築しています。
また、今後のバイオシミラー領域の売上目標ですが、現時点では2029年の150億円から修正していません。
海外事業

海外事業についてです。大きくASEANと米国に分けてご説明します。まず、ASEANでは4月から本格的に販売を開始した「Nextstellis」をポートフォリオの製品の核として、周りの製品を増やしていき、CDMO事業を伸ばしながらOLICの製販化に力を入れていきたいと考えています。
また、すでにお話ししましたが、米国向けに関しても、現在OLICと富士製薬工業本体の製剤開発のそれぞれで具体案が進んでいます。2024年9月期はこれを一層具体化し、着実に製品の供給を開始できるようにしたいと考えています。
これらを中心に、今期はASEANでの展開と米国市場へのアクセスをしっかり行いたいと考えていますが、米国市場へのアクセスに関しては、慎重に進めていくつもりです。
2023年9月期の総括と2024年9月期の対応

最後に、まとめとしてお話しします。今期事業計画達成の鍵は、「女性医療領域で必要とされる薬品を、いかに確実に患者さまに届けていくのか」ということに集約されると思いますので、この点について着実に手を打っていきます。
また、来期以降も国内でより一層患者さまのお役に立てるように、次のトップ製品として期待する「FSN-013」の確実な承認取得やバイオシミラーの新規承認申請、それらの周辺を固めるジェネリック製品の承認取得などを中心に進めていきます。さらに、海外ではASEAN、米国に事業を広げていきます。
本日ご説明したとおり、当社は従来はジェネリック企業として成長してきましたが、今期はより一層領域を特化したスペシャリティファーマ化を進めていきます。
2024年9月期株主還元
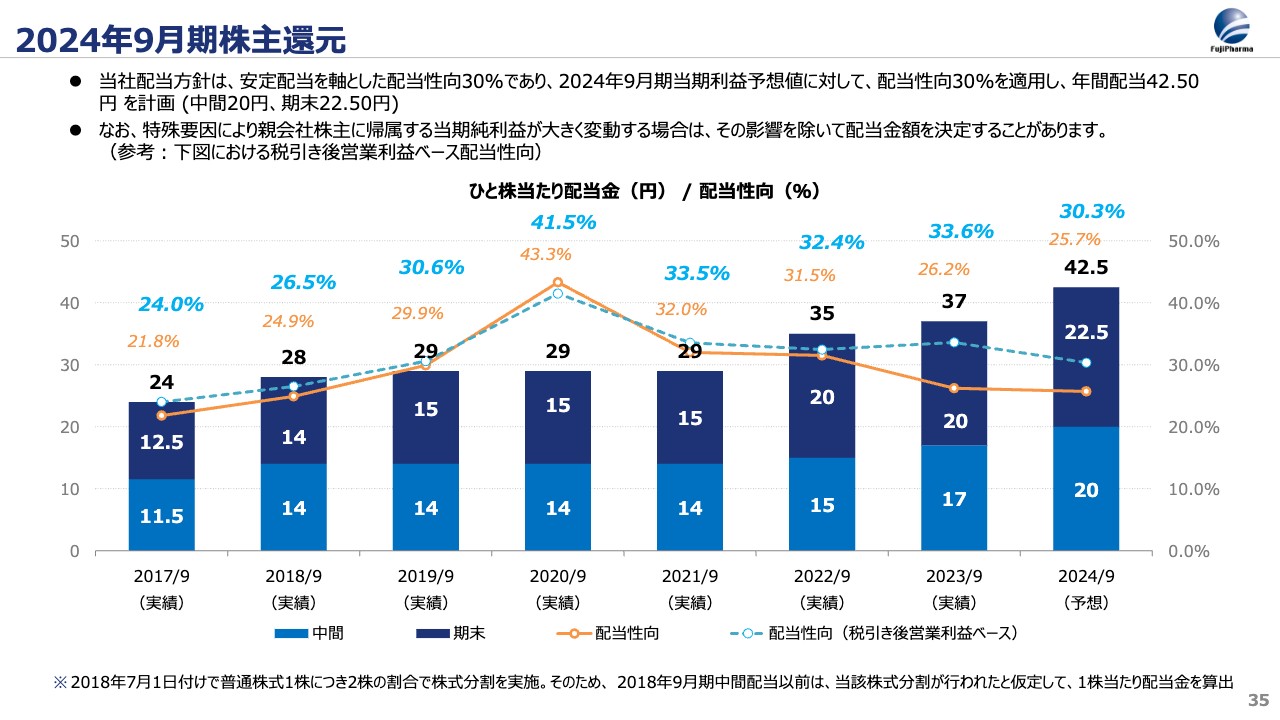
当社の配当方針としては、安定配当を軸として配当性向30パーセントを継続していきたいと考えています。2024年9月期の当期利益予想に対しても、特殊要因を除き配当性向30パーセントを適用し、年間配当42円50銭を計画しています。
質疑応答:新しい製剤棟について
司会者:「新しい製剤棟はすでに稼働していますか? 準備状況について教えてください」というご質問です。
森田周平氏(以下、森田):新しい製剤棟では、経口避妊薬を中心としたホルモン錠剤の製造を予定しています。現在の状況としては、製造設備や製造棟に必要な許可はすべて取得し、製造も完了しています。現在製造された製品の品質確認をしており、確認が取れ次第出荷の予定となっています。
質疑応答:緊急避妊薬の試験販売について
司会者:「緊急避妊薬の試験販売が開始されるそうですが、御社内で試験販売やOTC化への準備、対応は進んでいますか?」というご質問です。
岩井:緊急避妊薬の試験販売は、ちょうど今、業界誌や一般紙にも出てきています。
森田:岩井が話したとおり、先週の金曜日に厚生労働省から「医師の処方箋なしに緊急避妊薬を処方できる、薬局での試験販売が今月28日から始まる」と発表がありました。今後の方向性については、回答できる立場にないため控えますが、いかなる方向に進んだとしても、弊社として供給責任を果たせるように、今後の状況を注視しながら製造販売体制を整えていきたいと考えています。
質疑応答:「FSN-013」の適応症の申請について
司会者:「なぜ『FSN-013』は月経困難症だけ適用として申請したのでしょうか? 子宮内膜症性疼痛では申請しないのですか? また、申請しないことで影響はありますか?」というご質問です。
岩井:こちらは現在、研究開発部門で検討しています。
長縄:子宮内膜性疼痛の臨床試験の結果については、現在データを解析しており、その後で申請に向かうことも考えています。E4についてはいろいろなポテンシャルがあることから、製品価値を最大化するための取り組みを継続することも考えています。
質疑応答:「ウステキヌマブBS」の薬価収載を見送った理由について
司会者:「『ウステキヌマブBS』の薬価収載を見送った理由は何でしょうか?」というご質問です。
岩井:薬価収載を見送った理由は、海外製造所の生産計画をあらためて確認しているからです。安定供給することがとても大切になりますので、そこに支障がないよう、十分な量の在庫を確保し、問題なく上市できるかという確認です。
この結果、いったん延期することが必要と判断し、薬価収載を見送りました。ただし、何か生産に問題があったわけではなく、製造自体は順調に進んでいます。生産計画上の問題とご理解いただければと思います。
一方、補足的な内容になりますが、今年追加で3製剤の承認申請を計画していることをお伝えしました。これらへ影響があると不安になると思います。3製剤の開発は、新型コロナウイルスの影響等で、海外治験における患者さまのエントリーに若干遅れが出ていますが、開発そのものはおおむね計画どおりに進んでいます。いずれにしろ、安定供給を念頭にしっかりと開発・供給体制を整えていきたいと考えています。
質疑応答:バイオシミラーの開発進捗について

司会者:「バイオシミラーの開発進捗について、ProductB、ProductCの矢印の長さが、これまでの開示資料から変わっているのはなぜでしょうか?」というご質問です。
長縄:矢印の長さが変わっているのは、新型コロナウイルスあるいはグローバルのロジスティクスなどの影響によります。特に臨床試験に若干開発の遅れが出ている状況です。
質疑応答:初期臨床治験の廃止案について
司会者:「日本人の初期臨床治験廃止の案が出ましたが、御社の業績にプラスと捉えてもよいのでしょうか?」というご質問です。
岩井:我々も大変興味深くこの記事を見ています。
長縄:臨床試験においては、疾患ごとに開発ガイドラインがあるため、一律に今回の廃止案がプラスに働くかどうかの判断は現時点では難しいと考えています。今後は個別の開発案件について当局と相談しながら開発を進めていき、一刻も早く患者さまのもとに医薬品を提供できるように努力していきたいと考えています。
スポンサードリンク

