Buzzreach、FWD富士生命とがん患者に向けた治験情報提供をITネットワーク連携で開始
配信日時: 2020-10-05 11:00:19
製薬企業と患者を直接つなぐ治験情報インフラを展開している株式会社Buzzreach(本社:東京都品川区、代表取締役CEO:猪川 崇輝、以下Buzzreach)は、FWD富士生命保険株式会社(本社:東京都中央区、代表取締役社長兼 CEO:友野紀夫、以下FWD富士生命)とがん患者に向けたITネットワーク連携による、がん領域(オンコロジー)の治験情報提供を日本で初めて11月より開始することをお知らせいたします。
Buzzreachでは、今年4月より、がんに特化したサービスや情報提供を行う患者支援団体、患者会、ウェブメディアやSNSアプリ運営企業と業務提携をおこない、API*連携で製薬企業などから登録される治験情報を提供し、IT連携することで、より多くのがん患者やその家族に治験情報を届けるスキームを構築してまいりました。
FWD富士生命では、がんの「治療」だけではなく、その「生活」もサポートすることをコンセプトにした無解約返戻金型がん保険「FWD がんベスト・ゴールド」を11月2日より発売します。
また、この連携により、同日に日本全国で実施中のがん治験情報を検索できる業界初**のサービス「FWD がん治験情報提供サービス」を商品付帯サービスとして提供されます。
現在、がん治療薬は各製薬企業が進める開発品目の中心にあります。平成30年度のPmda(独立行政法人医薬品医療機器総合機構)報告***では全764本の治験届けのうち、343本が抗悪性腫瘍薬となっており、製薬企業と患者の双方のニーズが高まっております。当社が提供する治験情報マッチングプラットフォーム「smt (エス・エム・ティ)」ではこれまで、中枢神経系や希少疾患、小児疾患を中心に治験情報を提供しておりましたが、この度、がん領域の治験情報を新たに加えることで、製薬企業と患者、治験に携わっていない医師などに向け、不足している治験情報ニーズに合わせた情報提供の拡大をおこなうと同時に、日本初となるがん保険との連携でがんと宣告された被保険者およびご家族に対して、希望の一つである新たな治療の選択肢を提供できるようになります。
*API:Application Programming Interfaceの略称で、あるコンピュータプログラム(ソフトウェア)の機能や管理するデータなど、外部の他のプログラムから呼び出して利用するための手順やデータ形式などを定めた規約
**2020年9月時点 FWD 富士生命調べ
***Pmda(独立行政法人医薬品医療機器総合機構)報告 https://www.pmda.go.jp/files/000230480.pdf
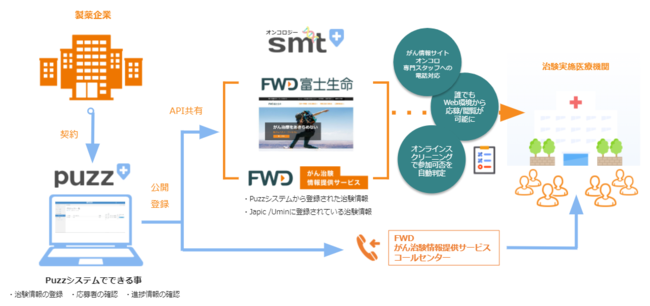
【サービスの展開図】
[画像1: https://prtimes.jp/i/36622/9/resize/d36622-9-173241-7.png ]
■Buzzreachの事業内容
治験(臨床試験・臨床研究)の様々な課題を解決するSaaSサービス
puzz(パズ) http://www.buzzreach.co.jp/lp/puzz/
製薬企業やアカデミア、医師主導で行われる治験を含む臨床試験、臨床研究の様々な課題を解決する機能が搭載されたSaaS型の管理システムです。
[画像2: https://prtimes.jp/i/36622/9/resize/d36622-9-236828-1.png ]
1.フィージビリティ・施設選定支援機能
治験を筆頭とした臨床試験、臨床研究のフィージビリティ調査、施設選定業務をサポートする機能。調査依頼から集計、選定までの業務の全てをオンラインで完結でき、調査後、試験実施後の施設情報はデータベース化することが可能。また、調査依頼先の新規紹介やマッチングも可能です。
2.プロジェクト(試験)運用/運用管理機能
施設選定後の施設アクティベイト管理から始まり、各施設の候補患者状況の視覚化をプランと比較しリアルタイムに把握が可能。
施設毎のスクリーニング情報を元にした候補患者の状況が視覚化されるため、被験者募集プランや施設追加、期間延長などの計画がより戦略的に立てることが可能になります。
3.治験情報公開・管理機能
製薬企業や臨床試験実施機関が主体となり治験を筆頭とした臨床試験情報を登録・公開・管理し、治験を主とした臨床試験情報を必要とする患者さんやご家族に向けて情報を提供、臨床試験実施医療機関の公開およびマッチング、参加申し込みまでをオンラインで完結できる製薬企業・研究者および医療機関向けの機能です。
治験(臨床試験・臨床研究)情報マッチングプラットフォーム
smt(エス・エム・ティ) https://www.searchmytrial.com/
[画像3: https://prtimes.jp/i/36622/9/resize/d36622-9-947310-2.png ]
新しい治療法や治療薬の情報を求める患者さんやご家族と日本にある全ての臨床試験情報をウェブ上でマッチングするサービスです。ご自身やご家族の環境や状況に合った治験情報だけでなく、近隣で、どの医療機関が該当する治験を実施するのかを知ることができます。製薬企業によってsmtに公開された治験情報は、治験実施医療機関の選択、参加申し込みまでをオンラインで完結できます。
また、様々な被験者募集環境(PRO、患者会、メディア)と連携が可能なため、多面的に被験者募集を実施する際の一元管理としても機能します。
治験(臨床試験・臨床研究)参加患者管理機能
[画像4: https://prtimes.jp/i/36622/9/resize/d36622-9-908737-5.png ]
患者(被験者)向け治験管理・リテンションアプリ
スタディ・コンシェルジュ https://www.buzzreach.co.jp/lp/msc/
治験参加患者に寄り添ったリアルタイムのコミュニケーションにより、治験参加患者の不安を和らげ、効率的に有効データを得ることで治験中止リスクを軽減し、新薬の早期承認を支援する業界初の画期的なアプリです。治験参加患者の治験薬の服薬忘れや飲みすぎを防ぎ、治験コーディネーター*(CRC:Clinical Research Coordinator)のサポート的な役割を担う治験管理アプリです。
*治験コーディネーターとは、製薬企業などによって開発された新薬が実際の薬として使用されるために必要な治験を含めた臨床研究を行う際に、医療機関や製薬会社、患者の間に立ち、スムーズに進行するようサポートするスタッフ。
smtの登録情報とITインフラを活用したsmt APIサービス
[画像5: https://prtimes.jp/i/36622/9/resize/d36622-9-389680-3.png ]
smt(エス・エム・ティ)では、治験情報の公開から実施医療機関への応募までワンストップで行えるインフラが整っており、製薬企業を中心とした自社のコーポレートサイトにペイシェントセントリシティの一環として、患者さん向けに治験情報を公開したい製薬企業や患者側の団体(患者会やメディア)などへ、当社のsmtの公開情報とインフラを提供できるAPIサービスです。
新型コロナウイルス(COVID-19)開発支援サイト
Covid-19 Cohort Study Site https://miilike.com/lp/covid-19/
[画像6: https://prtimes.jp/i/36622/9/resize/d36622-9-728314-4.png ]
Covid-19 Cohort Study Siteは、新型コロナウイルスに感染された方の体験談や新型コロナウイルスの治療薬・ワクチン開発(治験など)にご協力いただける方などの有志が集まることにより、治療薬・ワクチンの開発促進、そして新型コロナウイルス収束のために活かされます。
現在、全ての人にとって『見えない恐怖』でしかない新型コロナウイルスを、感染を体験された方々の貴重な声や確かな情報により、まずは『見える脅威』にしていくことが今求められています。感染拡大を止め、多くの命を救うために、コホート**への参加は非常に価値あるものとなります。
**コホート(cohort)とは、仲間のグループ。同一の属性を持つ集団。という意味を持ちます。『新型コロナウイルスをどうにかしたい』という、共通の因子を持ち、“集まっていただいた仲間”という意味で、コホートとしています。
会社概要
【会社名】株式会社Buzzreach
【設立年月日】2017年6月23日
【資本金】3億2,960万円(資本準備金含む)
【代表取締役CEO】猪川 崇輝
【所在地】東京都品川区上大崎2-15-19 MG目黒駅前
【HP】https://www.buzzreach.co.jp/
【事業内容】
・治験の様々な課題を解決するSaaSサービス
「puzz(http://www.buzzreach.co.jp/lp/puzz/)」の開発および販売
・患者(被験者)向け治験情報マッチングプラットフォーム
「smt(https://www.searchmytrial.com/)」の開発および販売
・患者(被験者)向け治験管理・リテンションアプリ
「スタディ・コンシェルジュ」(https://www.buzzreach.co.jp/lp/msc/)」の開発および販売
・臨床試験・製薬・ヘルスケア分野のグローバル企業向けBPO(ビジネスプロセスアウトソーシング)
PR TIMESプレスリリース詳細へ
スポンサードリンク
「バズリーチ」のプレスリリース
スポンサードリンク
最新のプレスリリース
- 国産“みどりまゆ”シルクブランド【絹生活研究所】、「肌トラブルとシルク化粧品のイメージ」アンケート結果を発表06/28 13:30
- eラーニング「ワークライフバランス」「レジリエンス」など10コースを2021年6月29日(火)に提供開始 06/28 13:30
- レーシングシミュレーターの開発・販売を手がけるZENKAIRACING.COMが『KYOJO CUP』に初参戦06/28 13:15
- 28cmサイズまで取り扱い!ヒール交換ができる最先端シューズ ヨーロッパ発シューズブランドの“Mime et moi”がEARLY SUMMER SUPERセールを開催!!06/28 13:15
- 旅行予約から旅行中の相談までがすべてオンラインで完結 アプリ『Holiday』オンライン旅行相談機能の正式開始06/28 13:00
- 最新のプレスリリースをもっと見る
